Gás nobre, qualquer um dos sete elementos químicos que compõem o Grupo 18 (VIIIa) da tabela periódica. Os elementos são hélio (He), néon (Ne), argônio (Ar), criptônio (Kr), xenônio (Xe), rádon (Rn) e oganesson (Og). Os gases nobres são gases incolores, inodoro, insípido e não inflamável. Tradicionalmente, eles foram rotulados como Grupo 0 na tabela periódica porque, décadas após a descoberta, acreditava-se que eles não podiam se relacionar com outros átomos; isto é, que seus átomos não poderiam combinar com os de outros elementos para formar compostos químicos. Suas estruturas eletrônicas e a constatação de que alguns deles realmente formam compostos levaram à designação mais apropriada, o Grupo 18.
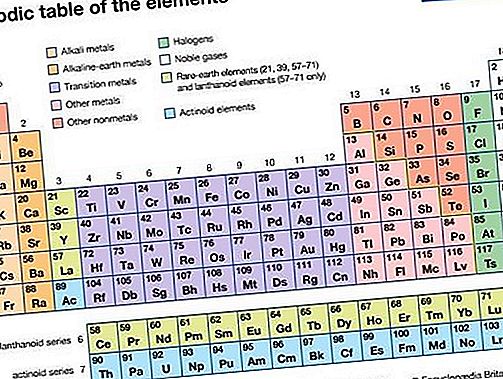
Quando os membros do grupo foram descobertos e identificados, eles foram considerados extremamente raros, além de quimicamente inertes e, portanto, foram chamados de gases raros ou inertes. Sabe-se agora, no entanto, que vários desses elementos são bastante abundantes na Terra e no resto do universo, de modo que a designação rara é enganosa. Da mesma forma, o uso do termo inerte tem a desvantagem de conotar passividade química, sugerindo que os compostos do Grupo 18 não possam ser formados. Na química e na alquimia, a palavra nobre há muito significa a relutância de metais, como ouro e platina, em sofrer reações químicas; aplica-se no mesmo sentido ao grupo de gases aqui coberto.
A abundância dos gases nobres diminui à medida que seus números atômicos aumentam. O hélio é o elemento mais abundante do universo, exceto o hidrogênio. Todos os gases nobres estão presentes na atmosfera da Terra e, exceto o hélio e o radônio, sua principal fonte comercial é o ar, do qual são obtidos por liquefação e destilação fracionada. A maior parte do hélio é produzido comercialmente a partir de certos poços de gás natural. O rádon normalmente é isolado como um produto da decomposição radioativa de compostos de rádio. Os núcleos dos átomos de rádio decaem espontaneamente emitindo energia e partículas, núcleos de hélio (partículas alfa) e átomos de radônio. Algumas propriedades dos gases nobres estão listadas na tabela.
Algumas propriedades dos gases nobres
| hélio | néon | argônio | krypton | xenon | radão | ununoctium | |
|---|---|---|---|---|---|---|---|
| * Em 25,05 atmosferas. | |||||||
| ** hcp = hexagonal compactado, fcc = cúbico centralizado na face (cúbico compactado). | |||||||
| *** Isótopo mais estável. | |||||||
| número atômico | 2 | 10 | 18 | 36. | 54 | 86 | 118 |
| peso atômico | 4,003 | 20.18 | 39.948 | 83,8 | 131.293 | 222 | 294 *** |
| ponto de fusão (° C) | -272,2 * | −248,59 | -189,3 | −157,36 | -111,7 | -71 | - |
| ponto de ebulição (° C) | −268,93 | −246,08 | -185,8 | -153,22 | -108 | -61,7 | - |
| densidade a 0 ° C, 1 atmosfera (gramas por litro) | 0,17847 | 0.899 | 1,784 | 3,75 | 5.881 | 9,73 | - |
| solubilidade em água a 20 ° C (centímetros cúbicos de gás por 1.000 gramas de água) | 8.61 | 10,5 | 33,6 | 59,4 | 108,1 | 230 | - |
| abundância isotópica (terrestre, por cento) | 3 (0,000137), 4 (99,999863) | 20 (90,48), 21 (0,27), 22 (9,25) | 36 (0,3335), 40 (99,6003) | 78 (0,35), 80 (2,28), 82 (11,58), 83 (11,49), 84 (57), 86 (17,3) | 124 (0,09), 126 (0,09), 128 (1,92), 129 (26,44), 130 (4,08), 131 (21,18), 132 (26,89), 134 (10,44), 136 (8,87) | - | - |
| isótopos radioativos (números de massa) | 5-10 | 16-19, 23-34 | 30-35, 37, 39, 41-53 | 69–77, 79, 81, 85, 87–100 | 110-125, 127, 133, 135-147 | 195-228 | 294 |
| cor da luz emitida pelo tubo de descarga gasosa | amarelo | vermelho | vermelho ou azul | amarelo verde | azul para verde | - | - |
| calor de fusão (quilojoules por mole) | 0,02 | 0,34 | 1,18 | 1,64 | 2.3 | 3 | - |
| calor de vaporização (calorias por mole) | 0,083 | 1,75 | 6.5 | 9,02 | 12,64 | 17 | - |
| calor específico (joules por grama de Kelvin) | 5.1931 | 1.03 | 0,52033 | 0,24805 | 0,15832 | 0,09365 | - |
| temperatura crítica (K) | 5.19 | 44,4 | 150,87 | 209,41 | 289,77 | 377 | - |
| pressão crítica (atmosferas) | 2,24 | 27,2 | 48,34 | 54,3 | 57,65 | 62 | - |
| densidade crítica (gramas por centímetro cúbico) | 0,0696 | 0,4819 | 0,5356 | 0,9092 | 1,103 | - | - |
| condutividade térmica (watts por metro Kelvin) | 0,1513 | 0,0491 | 0,0177 | 0,0094 | 0,0057 | 0,0036 | - |
| suscetibilidade magnética (unidades cgs por mole) | -0,0000019 | -0,0000072 | -0,0000194 | -0,000028 | -0,000043 | - | - |
| estrutura de cristal** | hcp | fcc | fcc | fcc | fcc | fcc | - |
| raio: atômico (angstroms) | 0,31 | 0,38 | 0,71 | 0,88 | 1.08 | 1.2 | - |
| raio: covalente (cristal) estimado (angstroms) | 0,32 | 0,69 | 0,97 | 1.1 | 1.3 | 1,45 | - |
| polarização estática (angstroms cúbicos) | 0,204 | 0,392 | 1,63 | 2.465 | 4.01 | - | - |
| potencial de ionização (primeiro, elétron-volts) | 24.587 | 21.565 | 15.759 | 13.999 | 12.129 | 10,747 | - |
| eletronegatividade (Pauling) | 4.5 | 4.0 | 2.9 | 2.6 | 2,25 | 2.0 | - |