Francium (Fr), elemento químico mais pesado do grupo 1 (Ia) da tabela periódica, o grupo dos metais alcalinos. Existe apenas em formas radioativas de curta duração. O francium natural não pode ser isolado em quantidades visíveis e pesáveis, pois apenas 24,5 gramas (0,86 onças) ocorrem a qualquer momento em toda a crosta terrestre. A existência de francium foi prevista pelo químico russo Dmitry I. Mendeleyev em sua classificação periódica dos elementos. A química francesa Marguerite Perey descobriu o francium (1939) enquanto estudava o actinium-227, que decai por decaimento beta negativo (emissão de elétrons) em um isótopo de tório (thorium-227) e por emissão alfa (cerca de 1%) em um isótopo de francium (francium-223) que era anteriormente chamado de actinium K (AcK) e é um membro da série de decaimento de actinium. Embora seja o isótopo de vida mais longa do francium, o francium-223 tem uma meia-vida de apenas 22 minutos. Trinta e quatro isótopos de hélio com massas entre 199 e 232 foram artificialmente preparados e, como o hélio natural não pode ser concentrado, ele também é preparado pela irradiação de nêutrons do rádio para produzir actínio, que decai para produzir traços de hélio. A química do francium pode ser estudada apenas por métodos projetados para quantidades vestigiais. Em todos os aspectos, seu comportamento observado, incluindo o estado de oxidação de +1, é o esperado de um elemento alcalino preenchendo um local logo abaixo do césio na tabela periódica dos elementos. Quase não há informações sobre seus aspectos biológicos.
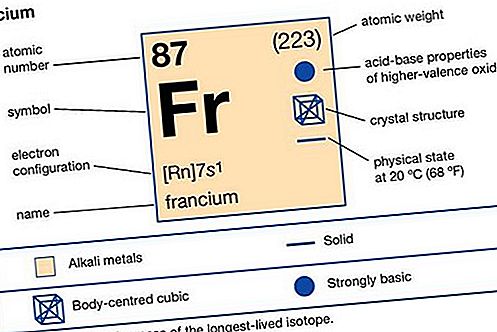

metal alcalino
césio (Cs) e francium (Fr). Os metais alcalinos são assim chamados porque a reação com a água forma álcalis (isto é, bases fortes capazes de
.Propriedades do elemento
| número atômico | 87 |
|---|---|
| isótopo mais estável | (223) |
| Estado de oxidação | +1 |
| configuração eletrônica | 2-8-18-32-18-8-1 ou [Rn] 7s 1 |













