Urânio (U), elemento químico radioativo da série actinóide da tabela periódica, número atômico 92. É um combustível nuclear importante.
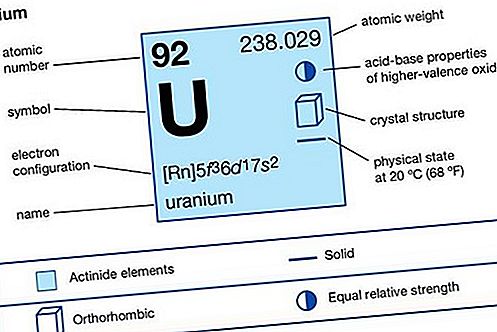

elemento actinóide
os membros do grupo, incluindo o urânio (o mais familiar), ocorrem naturalmente, a maioria é feita pelo homem. Tanto o urânio quanto o plutônio foram utilizados
O urânio constitui cerca de duas partes por milhão da crosta terrestre. Alguns minerais importantes de urânio são pitchblenda (U 3 O 8 impuro), uraninita (UO 2), carnotita (vanadato de urânio potássico), autunita (fosfato de cálcio e urânio) e torbernita (fosfato de cobre e urânio). Esses e outros minérios de urânio recuperáveis, como fontes de combustíveis nucleares, contêm muitas vezes mais energia do que todos os depósitos recuperáveis conhecidos de combustíveis fósseis. Um quilo de urânio produz tanta energia quanto 1,4 milhão de quilos (3 milhões de libras) de carvão.
Para obter informações adicionais sobre depósitos de minério de urânio, bem como cobertura de técnicas de mineração, refino e recuperação, consulte Processamento de urânio. Para dados estatísticos comparativos sobre a produção de urânio, consulte a tabela.
Urânio
| país | produção de minas 2013 (toneladas) | % da produção mundial de minas |
|---|---|---|
| *Estimativa. | ||
| Fonte: Associação Nuclear Mundial, Produção Mundial de Mineração de Urânio (2014). | ||
| Cazaquistão | 22.574 | 37,9 |
| Canadá | 9.332 | 15,6 |
| Austrália | 6.350 | 10,6 |
| Níger* | 4.528 | 7.6 |
| Namíbia | 4.315 | 7.2 |
| Rússia | 3.135 | 5.3 |
| Usbequistão * | 2.400 | 4.0 |
| Estados Unidos | 1.835 | 3.1. |
| China* | 1.450 | 2.4 |
| Malawi | 1.132 | 1.9 |
| Ucrânia | 1.075 | 1.9 |
| África do Sul | 540 | 0,9 |
| Índia* | 400 | 0,7 |
| República Checa | 225 | 0,4 |
| Brasil | 198 | 0,3 |
| Romênia * | 80 | 0,1 |
| Paquistão* | 41. | 0,1 |
| Alemanha | 27 | 0,0 |
| total mundial | 59.637 | 100 |
O urânio é um elemento metálico denso e duro, de cor branca prateada. É dúctil, maleável e capaz de dar um alto polimento. No ar, o metal fica manchado e, quando finamente dividido, quebra em chamas. É um condutor de eletricidade relativamente ruim. Embora descoberto (1789) pelo químico alemão Martin Heinrich Klaproth, que o nomeou em homenagem ao então recentemente descoberto planeta Urano, o próprio metal foi isolado pela primeira vez (1841) pelo químico francês Eugène-Melchior Péligot pela redução do tetracloreto de urânio (UCl 4) com potássio.
A formulação do sistema periódico pelo químico russo Dmitry Mendeleyev, em 1869, concentrou a atenção no urânio como o elemento químico mais pesado, posição que manteve até a descoberta do primeiro elemento transurânio neptúnio em 1940. Em 1896, o físico francês Henri Becquerel descobriu no urânio. o fenômeno da radioatividade, termo usado pela primeira vez em 1898 pelos físicos franceses Marie e Pierre Curie. Esta propriedade foi encontrada posteriormente em muitos outros elementos. Sabe-se agora que o urânio, radioativo em todos os seus isótopos, consiste naturalmente de uma mistura de urânio-238 (99,27%, meia-vida de 4.510.000.000 anos), urânio-235 (0,72%, meia-vida de 713.000.000 anos) e urânio-234 (0,006%, meia-vida de 247.000 anos). Essas meias-vidas longas tornam possíveis as determinações da idade da Terra, medindo as quantidades de chumbo, o produto final de decaimento do urânio, em certas rochas que contêm urânio. O urânio-238 é o pai e o urânio-234, uma das filhas da série de decaimento radioativo do urânio; O urânio-235 é o pai da série de decaimento de actínio. Veja também elemento actinóide.
O elemento urânio tornou-se objeto de intenso estudo e amplo interesse depois que os químicos alemães Otto Hahn e Fritz Strassmann descobriram no final de 1938 o fenômeno da fissão nuclear em urânio bombardeado por nêutrons lentos. O físico americano nascido na Itália, Enrico Fermi, sugeriu (início de 1939) que os nêutrons poderiam estar entre os produtos de fissão e, portanto, poderiam continuar a fissão como uma reação em cadeia. O físico norte-americano húngaro Leo Szilard, o físico americano Herbert L. Anderson, o químico francês Frédéric Joliot-Curie e seus colegas de trabalho confirmaram (1939) essa previsão; investigação posterior mostrou que uma média de 2 1 / 2 neutrões por átomo são libertados durante fissão. Essas descobertas levaram à primeira reação em cadeia nuclear autossustentável (2 de dezembro de 1942), ao primeiro teste de bomba atômica (16 de julho de 1945), à primeira bomba atômica lançada em guerra (6 de agosto de 1945), a primeira bomba atômica. submarino (1955) e o primeiro gerador elétrico em escala nuclear (1957).
A fissão ocorre com nêutrons lentos no isótopo relativamente raro urânio-235 (o único material físsil que ocorre naturalmente), que deve ser separado do abundante isótopo urânio-238 para seus vários usos. O urânio-238, no entanto, após absorver nêutrons e sofrer decaimento beta negativo, é transmutado no elemento sintético plutônio, que é físsil com nêutrons lentos. O urânio natural, portanto, pode ser usado em reatores conversores e reprodutores, nos quais a fissão é sustentada pelo raro urânio-235 e o plutônio é fabricado ao mesmo tempo pela transmutação de urânio-238. O urânio físsil-233 pode ser sintetizado para uso como combustível nuclear a partir do isótopo não-físsil de tório tório-232, que é abundante na natureza. O urânio também é importante como material primário a partir do qual os elementos sintéticos do transurânio foram preparados por reações de transmutação.
O urânio, que é fortemente eletropositivo, reage com a água; dissolve-se em ácidos, mas não em álcalis. Os estados de oxidação importantes são +4 (como no óxido UO 2, tetra-halogenetos como UCl 4 e o íon aquoso verde U 4 +) e +6 (como no óxido UO 3, hexafluoreto UF 6 e uranil amarelo íon UO 2 2+). Em uma solução aquosa, o urânio é mais estável que o íon uranil, que possui uma estrutura linear [O = U = O] 2+. O urânio também exibe um estado +3 e +5, mas os respectivos íons são instáveis. O íon U 3+ vermelho oxida lentamente mesmo em água que não contém oxigênio dissolvido. A cor do íon UO 2 + é desconhecida, pois sofre desproporcionalidade (o UO 2 + é simultaneamente reduzido a U 4 + e oxidado a UO 2 2+), mesmo em soluções muito diluídas.
Os compostos de urânio têm sido utilizados como corantes para a cerâmica. O hexafluoreto de urânio (UF 6) é um sólido com uma pressão de vapor invulgarmente alta (115 torr = 0,15 atm = 15 300 Pa) a 25 ° C (77 ° F). O UF 6 é quimicamente muito reativo, mas, apesar de sua natureza corrosiva no estado de vapor, o UF 6 tem sido amplamente utilizado nos métodos de difusão e centrífuga de gás para separar o urânio-235 do urânio-238.
Os compostos organometálicos são um grupo interessante e importante de compostos nos quais existem ligações metal-carbono ligando um metal a grupos orgânicos. Uranocene é um composto organouranium L (C 8 H 8) 2, em que um átomo de urânio é ensanduichada entre duas camadas de anéis orgânicas relacionadas com ciclo-octatetraeno C 8 H 8. Sua descoberta em 1968 abriu uma nova área de química organometálica.
Propriedades do elemento
| número atômico | 92 |
|---|---|
| peso atômico | 238,03 |
| ponto de fusão | 1.132,3 ° C (2.070,1 ° F) |
| ponto de ebulição | 3.818 ° C (6.904 ° F) |
| Gravidade Específica | 19.05 |
| estados de oxidação | +3, +4, +5, +6 |
| configuração eletrônica do estado atômico gasoso | [Rn] 5f 3 6d 1 7s 2 |









![Batalha de Cowpens Revolução Americana [1781] Batalha de Cowpens Revolução Americana [1781]](https://images.thetopknowledge.com/img/world-history/4/battle-cowpens-american-revolution-1781.jpg)

