Polônio (Po), um elemento metálico radioativo, cinza-prateado ou preto do grupo oxigênio (Grupo 16 [VIa] na tabela periódica). O primeiro elemento a ser descoberto por análise radioquímica, o polônio foi descoberto em 1898 por Pierre e Marie Curie, que estavam investigando a radioatividade de uma certa pitchblenda, um minério de urânio. A radioatividade muito intensa, não atribuível ao urânio, foi atribuída a um novo elemento, nomeado por eles em homenagem à terra natal de Marie Curie, na Polônia. A descoberta foi anunciada em julho de 1898. O polônio é extremamente raro, mesmo em pitchblende: 1.000 toneladas de minério devem ser processadas para obter 40 miligramas de polônio. Sua abundância na crosta terrestre é de cerca de uma parte em 10 15. Ocorre na natureza como um produto de decaimento radioativo de urânio, tório e actínio. A meia-vida de seus isótopos varia de uma fração de segundo a 103 anos; o isótopo natural mais comum do polônio, o polônio-210, tem uma meia-vida de 138,4 dias.
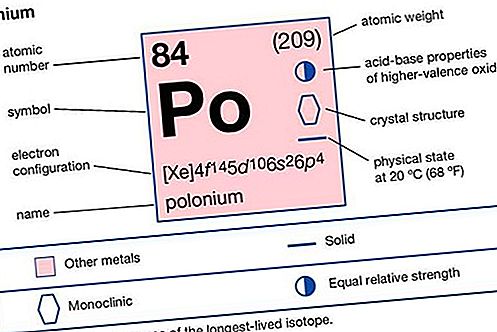
O polônio geralmente é isolado de subprodutos da extração de rádio de minerais de urânio. No isolamento químico, o minério de pitchblenda é tratado com ácido clorídrico e a solução resultante é aquecida com sulfeto de hidrogênio para precipitar o monossulfeto de polônio, PoS, juntamente com outros sulfetos metálicos, como o bismuto Bi 2 S 3, que se assemelha ao monossulfeto de polônio intimamente em comportamento químico, embora seja menos solúvel. Devido à diferença de solubilidade, a precipitação parcial repetida da mistura de sulfetos concentra o polônio na fração mais solúvel, enquanto o bismuto se acumula nas porções menos solúveis. A diferença de solubilidade é pequena, no entanto, e o processo deve ser repetido várias vezes para obter uma separação completa. A purificação é realizada por deposição eletrolítica. Pode ser produzido artificialmente bombardeando o bismuto ou chumbo com nêutrons ou com partículas carregadas aceleradas.
Quimicamente, o polônio se assemelha aos elementos telúrio e bismuto. São conhecidas duas modificações do polônio, as formas α e β, ambas estáveis à temperatura ambiente e com características metálicas. O fato de sua condutividade elétrica diminuir à medida que a temperatura aumenta coloca o polônio entre os metais, em vez dos metalóides ou não metais.
Como o polônio é altamente radioativo - desintegra-se a um isótopo estável de chumbo emitindo raios alfa, que são fluxos de partículas carregadas positivamente -, ele deve ser tratado com extremo cuidado. Quando contido em substâncias como a folha de ouro, que impede a radiação alfa de escapar, o polônio é usado industrialmente para eliminar a eletricidade estática gerada por processos como laminação de papel, fabricação de chapas plásticas e fiação de fibras sintéticas. Também é usado em pincéis para remover poeira de filmes fotográficos e na física nuclear como fonte de radiação alfa. Misturas de polônio com berílio ou outros elementos leves são usadas como fontes de nêutrons.
Propriedades do elemento
| número atômico | 84 |
|---|---|
| peso atômico | 210. |
| ponto de fusão | 254 ° C (489 ° F) |
| ponto de ebulição | 962 ° C (1.764 ° F) |
| densidade | 9,4 g / cm 3 |
| estados de oxidação | −2, +2, +3 (?), +4, +6 |
| configuração eletrônica | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 10 6s 2 6p 4 |